65歳以上の成人に対する肺炎球菌ワクチン接種に関する考え方(第3版 2019-10-30)
65歳以上の成人に対する肺炎球菌ワクチン接種に関する考え方(2019年~2023年の接種)
<内容>
1)はじめに
2)PPSV23の定期接種について
3)成人におけるPCV13の位置づけ
4)PCV13-PPSV23連続接種の考え方
5)合同委員会の見解
6)PPSV23とPCV13の併用接種時の接種間隔に関する考え方
7)定期接種としての肺炎球菌ワクチン接種の考え方
8)おわりに
資料1.海外の予防接種制度
参考文献
1)はじめに
2014年10月1日より23価肺炎球菌莢膜ポリサッカライドワクチン(PPSV23)の65歳以上の成人を対象とした予防接種法に基づく定期接種が開始され、65歳の者及び60歳以上65歳未満で心臓、腎臓又は呼吸器の機能に自己の身辺の日常生活活動が極度に制限される程度の障害を有する者及びヒト免疫不全ウイルスにより免疫の機能に日常生活がほとんど不可能な程度の障害を有する者を対象に、PPSV23を1回接種とすることとなった。また、2014年10月〜2019年3月までの期間における時限措置として、各年度に65歳、70歳、75歳、80歳、85歳、90歳、95歳および100歳となる者(2014年度については100歳以上になる者を含む)を接種対象とした。その後、2019年1月10日に開催された第27回厚生科学審議会予防接種・ワクチン分科会予防接種基本方針部会において、2019年度以降も5年間の時限措置を継続することが決定された1)。
一方、2014年6月に13価肺炎球菌結合型(PCV13)が、65歳以上の成人に適応拡大されたことから、PCV13を同対象年齢に対して任意接種ワクチンとして接種することが可能となった。2014年9月に米国Advisory Committee on Immunization Practices; ACIP)は、65歳以上の成人に対するPPSV23, PCV13両方を定期接種とし、これらを連続接種することを推奨した2)。尚、米国ACIPはこの連続接種の推奨については2018年に見直すとした。
このような背景から、日本呼吸器学会ワクチン検討WG委員会及び日本感染症学会ワクチン委員会はその合同委員会を組織し、現時点での「65歳以上の成人に対する肺炎球菌ワクチン接種の考え方(以下、「考え方」とする)を実地臨床医家に対し公表してきた(2015年1月に「考え方」第1版、2017年10月に「考え方」第2版)。この中で、合同委員会としては2014年の米国ACIPによるPCV13-PPSV23連続接種の推奨を全面的には受け入れるべきではないとしてきたところである。
その後、2018年10月31日開催の第24回厚生科学審議会予防接種・ワクチン分科会予防接種基本方針部会において、PCV13の定期接種化の可能性について審議された。同部会ではPCV13を65歳以上の成人に対する定期接種に指定するメリットは少ないと結論された3)。一方、2019年6月に開催された米国ACIP会議において、1)65歳以上の成人に対するPCV13接種の推奨について協議され、PCV13接種歴のない、免疫不全を有しない65歳以上の成人に対して症例毎の臨床判断注1に基づいたPCV13接種の推奨が承認された4)。 しかしながら、2)全ての65歳以上の成人に対するPCV13の接種とPCV13-PPSV23連続接種の推奨については承認されなかった。尚、3)全ての65歳以上の成人に対するPPSV23接種の推奨は承認された(注1 原文ではShared clinical decision making:Shared decision makingの日本語訳には、共有意思決定、協働的意思決定などがあてられている)。このような2014年以降のわが国及び米国ACIPによる65歳以上の成人に対する肺炎球菌ワクチンの推奨の内容を鑑み、「考え方」を改訂する。
2)PPSV23の定期接種について
PPSV23 (ニューモバックスNPⓇ)は1988年に薬事承認された。2014年10月1日より65歳以上の成人を対象としたPPSV23の定期接種(B類疾病)が開始された。その後、2018年5月にアップデートされたPPSV23のファクトシートが公表され5)、PPSV23の65歳以上の成人に対するワクチン効果についての以下のエビデンスが明らかにされている。
PPSV23の定期接種導入前の2011年9月から2014年8月の期間に国内でtest-negative designによって実施された多施設前向き研究において、65歳以上の高齢者における市中発症肺炎に対するPPSV23のワクチン効果が報告された6)。5年以内のPPSV23接種のワクチン効果はすべての肺炎球菌性肺炎に対して27.4%、ワクチン血清型の肺炎球菌性肺炎に対して33.5%であった。
さらに、成人の侵襲性肺炎球菌感染症(IPD)サーベイランスにおいて、PPSV23接種のIPDに対するワクチン効果が報告された。全年齢層のPPSV23ワクチン血清型によるIPDに対するワクチン効果は45%であり、65歳以上におけるワクチン効果は39%であった7)
しかしながら、2014〜17年度における65歳以上の成人のPPSV23の接種率は30%台に留まっていることから8)、前述のように2019年度以降の5年間は時限措置を継続することが決定された。
3)成人におけるPCV13の位置づけ
2015年7月にPCV13(成人用)ファクトシートが公表された。本ファクトシートでは、以下のエビデンスが示されている。海外データ及び国内データから、65歳以上の成人に対するPCV13の安全性はPPSV23とほぼ同等、またPCV13の免疫原性は同等もしくはPPSV23より優れている9-11)。また、PCV13は65歳以上の成人におけるワクチン含有型の侵襲性肺炎球菌感染症(IPD)のみならず菌血症を伴わない肺炎球菌性肺炎を有意に減少させたと報告されている12)。
厚生労働省研究班「成人の侵襲性細菌感染症サーベイランスの構築に関する研究」(2016〜18年度)において、2013年4月〜2018年3月の期間に成人IPD原因菌 (n=1,277株)の血清型分布が検討された13)。2013〜2015年度におけるIPD原因菌のPCV13とPPSV23による血清型カバー率はそれぞれ41〜48%, 65〜68%であった。一方、2016〜2017年度ではPCV13の血清型カバー率は31%に低下したのに対し、PPSV23の血清型カバー率は65%と変化がなかった。全国からIPD原因菌を収集して解析したUbukataらの研究でも、PCV13含有血清型による成人のIPDの割合は、2010年度の74.1%から2016年度には37.7%に減少していた。一方、PPSV23に含まれPCV13に含まれない血清型による成人IPDの割合は、2010年度の12.4%から徐々に増加し2016年度には33.6%に達していた14)
また、Sandoらはわが国で、2011年から2014年(I相)と2016年から2017年(II相)に国内の5つの医療機関で成人の肺炎球菌性肺炎の疫学調査を実施し、原因菌の血清型分布の研究期間での違いを比較した(第I相241例、第II相243例)。その結果、PCV13含有血清型の占める割合は、53%から33%に減少していたが、PPSV23含有血清型(PCV13含有血清型を除く)に変化は認められなかった15)。また、単一医療機関における成人の肺炎球菌性肺炎の原因菌229株の血清型解析においても、2011年から2015年の期間におけるPCV13とPPSV23による血清型カバー率はそれぞれ71.4%から33.3%,71.4%から50%まで減少した16)。しかし、2016年と2017年においては、PCV13による血清型カバー率はそれぞれ37.5%と32.4%、PPSV23によるカバー率は54.2%と47.1%であり、2015年から2017年の期間においては概ね変化はみられなかった17)。
欧州での肺炎球菌ワクチンの医療経済学的解析では、PPSV23単回接種は2万ユーロ/QALY未満であるのに対し、PCV13単回接種は10万ユーロ/QALYであり、PPSV23単回接種の方が費用対効果は良好としている18)。一方、AMED研究班による国内疫学データを踏まえた医療経済学的解析では、PCV13の単回接種(334万円/QALY)の費用対効果はPPSV23単回接種(448万円/QALY)と比較してやや良好な結果であった5)。
2018年度の厚生科学審議会予防接種・ワクチン分科会予防接種基本方針部会において、65歳以上の成人におけるPCV13接種の安全性、ワクチン効果及び国内のIPDや肺炎原因菌の血清型分布などの検討から、PCV13は65歳以上の成人を対象とした定期接種ワクチンとしては位置づけないと結論された3)。
4)PCV13-PPSV23連続接種の考え方
米国ACIPは2014年9月にMorbidity and Mortality Weekly Report誌上で、PCV13、PPSV23を含む成人の肺炎球菌ワクチンの推奨について発表した。すなわち、米国ACIPはこれまでに肺炎球菌ワクチンの接種歴が無い、または接種歴不明の65歳以上の成人に対して、PCV13の初回接種後 6〜12か月の間隔でのPPSV23の追加接種(PCV13-PPSV23連続接種)を推奨した2)。このPCV13-PPSV23の連続接種の利点は、成人ではPCV13接種後に、被接種者に13血清型の莢膜抗原特異的なメモリーB細胞が誘導され、その後のPPSV23接種により両ワクチンに共通な12血清型に対する特異抗体のブースター効果が期待されることである。この連続接種により肺炎球菌ワクチンの予防効果を増強、拡大する可能性が期待される。しかしながら、PCV13は任意接種ワクチンであり、また短期間での連続接種の安全性は国内では確認されておらず、さらに連続接種による臨床効果のエビデンスは国内外を通じて示されていない。なお、2015年6月に米国ACIPは米国Center for Medicare & Medicaid Serviceのポリシーに基づいて、PCV13初回接種後のPPSV23の接種間隔を1年以上にすべき、と推奨内容を修正した19)。その後、前述の成人PCV13の追加接種に関する米国ACIPの推奨は費用対効果の点からも妥当だと判断する論文が報告された20)。
また、米国Center for Disease Control and Prevention (CDC)は2017年7月に、2009年9月19日から2016年9月18日の間に、65歳以上の成人の31.5%が少なくとも1回のPCV13接種を、18.3%がそれぞれ少なくとも1回のPCV13とPPSV23接種をしたことをMMWR誌上で報告している21)。
5)合同委員会の見解
1.第1版の「考え方」における見解(2015年1月)
65歳以上の成人に対するPCV13の免疫原性、安全性に関する国内・国外のデータは認められるが9-11)、臨床効果の成績はオランダにおける一報のみである12)。また、2014年当時はその費用対効果の解析も未実施であった。このため、合同委員会としては、現時点では65歳以上の成人におけるPCV13を含む肺炎球菌ワクチンのエビデンスに基づく指針を提示することは困難と判断した。また、2014年9月に米国ACIPは成人のPCV13-PPSV23連続接種の65歳以上の成人に対する推奨について発表した2)。尚、この65歳以上の成人に対するPCV13の推奨については2018年に再評価するとされていた。一方、米国でPCV13を定期接種とする根拠となった65歳以上の成人に対するPCV13の臨床効果、費用対効果の推定については、米国における65歳以上の成人における侵襲性肺炎球菌感染症(IPD)、肺炎球菌性肺炎の罹患率、原因血清型の分布等が利用されたと考えられる。しかしながら、わが国の成人におけるPCV13の背景は、小児におけるPCV7/PCV13の導入時期の違い等から、米国における背景とは異なると考えられる。このため、2015年1月の時点で合同委員会はわが国の肺炎球菌ワクチンに関する考え方に、米国ACIPのPCV13接種を含む推奨内容を全面的には取り入れるべきではないと判断した。一方、本合同委員会としては、わが国の実地臨床医家に対してPCV13接種の可能な選択肢を示すことが必要であるが、日本独自の臨床的、医療経済的エビデンスは確定していないため、主に安全性の観点から「65歳以上の成人における肺炎球菌ワクチン接種の考え方」として提示することとした。
2.第2版の「考え方」における見解(2017年10月)
2017年10月時点で、第1版の「考え方」を公開(2014年9月)後の65歳以上の成人に対するPCV13の臨床効果に関する追加情報はない。
わが国の成人におけるIPD原因菌及び65歳以上の成人の肺炎球菌性肺炎の原因菌のPCV13とPPSV23による血清型カバー率はいずれも不変またはやや減少傾向である。米国CDCが示した65歳以上の成人に対するPCV13追加接種の費用対効果の妥当性に関して、2014年時点での検討には、PCV13による小児定期接種導入の集団免疫効果(65歳以上の成人における肺炎球菌性肺炎患者数の減少)並びにPPSV23の65歳以上の成人における肺炎球菌性肺炎に対するワクチン効果(直接効果)が反映されていない。
以上より、本合同委員会としては、2017年10月時点においても米国ACIPのPCV13-PPSV23連続接種の推奨を全面的には受け入れるべきではないと結論した。
3.第3版の「考え方」における見解(2019年10月)
2018年度の厚生科学審議会予防接種ワクチン分科会において、65歳以上の成人に対してPPSV23による定期接種を継続し、2014〜2018年度に実施した5年経過措置を引き続き2019〜2023年度に実施することを決定した。また、同分科会は65歳以上の成人に対する定期接種としてはPCV13を位置づけないことを決定した。
一方、2019年6月に開催された米国ACIP会議において、65歳以上の成人に対するPCV13-PPSV23の連続接種は推奨されなかった4)。また、今回の米国ACIP会議資料にはPCV13-PPSV23の妥当性を示すデータは確認できなかったものの21)、合同委員会はPCV13-PPSV23連続接種の考え方自体が否定された訳ではないと考える。
このような背景から、合同委員会としては第3版の「考え方」において、第2版の「考え方」に引き続き、定期接種対象者がPPSV23の定期接種を受けられるよう接種スケジュールを決定することを推奨する。また、65歳以上の成人に対し、PCV13を接種後にPPSV23接種(定期接種もしくは任意接種)を受ける連続接種スケジュールについても可能な選択肢とする。
6)PPSV23とPCV13の併用接種時の接種間隔に関する考え方
①PPSV23の再接種間隔
PPSV23接種後5年以上の間隔をおいてPPSV23を再接種することが可能である23)。
②PCV13接種後のPPSV23の接種間隔
PCV13とPPSV23の接種間隔については、その安全性と両ワクチンに共通な血清型特異抗体のブースター効果が確認されている6か月から4年以内に行う24-28)ことが推奨される。それ以上の接種間隔を空けた場合、PPSV23によるブースター効果が得られるか否かについてはエビデンスが示されていない。
③PPSV23接種後のPCV13の接種間隔
PPSV23接種後のPCV13接種について、PCV13接種によって先行するPPSV23接種後以上の免疫応答は得られないものの、1年の間隔が保たれれば、その安全性には問題が無いことが確認されている24)。
7)定期接種としての肺炎球菌ワクチン接種の考え方
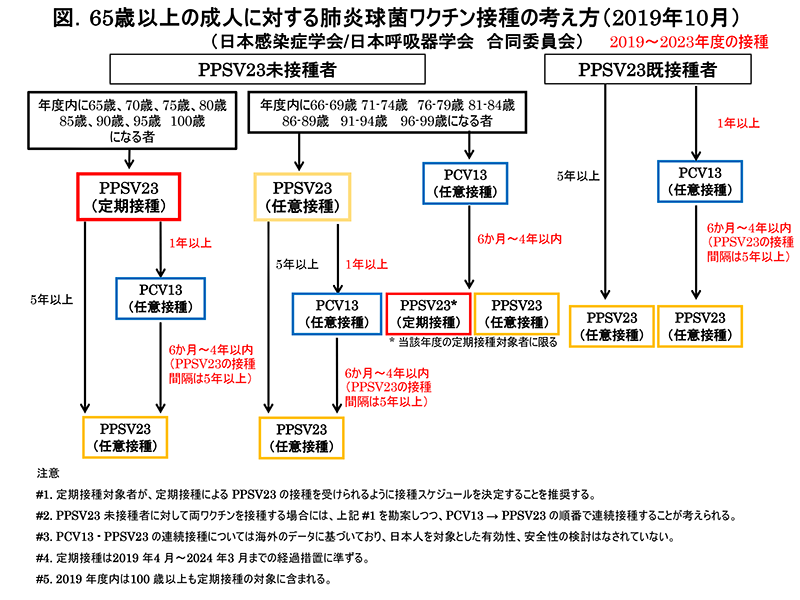
2019〜2023年度の接種について(図)
1.PPSV23未接種者について
- PPSV23の定期接種
PPSV23未接種で、2019〜2023年度に65歳、70歳、75歳、80歳、85歳、90歳、95歳、100歳となる者は、該当する年度にPPSV23の定期接種の対象となる。2019年度内は100歳以上の者も対象となる。PPSV23接種後5年以上の間隔をおいてPPSV23の再接種23)、もしくは1年以上の間隔をおいてPCV13-PPSV23の連続接種をすることも考えられる24)。PCV13とPPSV23の接種間隔については、6か月から4年が適切と考えられる24-28)。この場合もPPSV23の再接種間隔は5年以上が必要である。 - PPSV23の任意接種
PPSV23未接種で、当該年度の定期接種対象でない65歳以上の成人は、PPSV23を任意接種として接種できる。自治体によっては、65歳以上の成人に公費助成を行っている。PPSV23接種後5年以上の間隔をおいてPPSV23の再接種23)、 もしくは1年以上の間隔を置いてPCV13-PPSV23の連続接種をすることも考えられる24)。PCV13とPPSV23の接種間隔については、6か月から4年が適切と考えられる24-28)。この場合もPPSV23の再接種間隔は5年以上が必要である。
また、3回目、4回目の接種についても再接種と同程度の免疫原性と安全性が確認されている29)。このため症例によっては再接種を繰り返すことを考慮してよいと考える。 - PCV13の任意接種
PPSV23未接種で、2020〜2023年度の定期接種対象者については、PCV13の 任意接種を終了し、その6か月以降にPPSV23の定期接種あるいはPPSV23の 任意接種を受けることができる。PCV13接種後にPPSV23を接種する場合には、 6か月から4年の間隔が適切と考えられる24-28)。
2.PPSV23既接種者について
PPSV23既接種者は定期接種の対象外となる。PPSV23接種後5年以上の間隔をおいてPPSV23の再接種23)、もしくはPPSV23接種後1年以上の間隔をおいてPCV13の接種をすることも考えられる24)。PCV13接種後にPPSV23を再接種する場合には、6か月から4年の間隔が適切と考えられるが24-28)、それ以降でも接種可能である。この場合もPPSV23の再接種間隔は5年以上が必要である。
8)おわりに
小児におけるPCV7/PCV13の定期接種導入による間接効果により、成人の肺炎球菌感染症の罹患率及び原因菌の血清型分布が変化する中、本合同委員会は「65歳以上の成人に対する肺炎球菌ワクチンに関する考え方」(第3版)を示した。
2019年度以降も65歳以上の成人に対してPPSV23による定期接種の5年間の時限措置が継続される事が決定した。また、わが国ではPCV13を定期接種ワクチンに位置づけない方針となったが、PCV13-PPSV23の連続接種の考え方が完全に否定されている訳ではないことから、この連続接種スケジュールについても可能な選択肢とした。また、2014〜17年度における65歳以上の成人におけるPPSV23の接種率は30%台と低いことから8)、2019年度以降の5年時限措置の間にはPPSV23の接種率向上を目指すことが求められる。この「考え方」が実地臨床医家の65歳以上の成人に対する肺炎球菌ワクチン接種の参考になれば幸いである。
尚、この「考え方」においては、米国ACIPが推奨する免疫不全者におけるPCV13-PPSV23の連続接種については触れないこととした30)。
資料1.海外の予防接種制度
高齢者に対する肺炎球菌ワクチン接種に関する各国の対応は一律ではない。2019年6月に開催された米国ACIPにおいて、全ての65歳以上の成人に対するPPSV23接種の推奨は承認された。一方、PCV13接種歴のない、免疫不全を有しない65歳以上の成人に対して、症例毎の臨床判断に基づいたPCV13接種の推奨が承認された。また、全ての65歳以上の成人に対するPCV13の接種と3)PCV13-PPSV23連続接種の推奨については承認されなかった4)。
英国ではJCVI(Joint Committee on Vaccination and Immunization)がワクチン接種の方針を決めている。JCVIはPCV13の費用対効果分析において、良好な結果が見込まれないと判断し、PPSV23においては、この先数年で医療経済性は低下するかもしれないものの現時点では、依然として65歳以上の高齢者において、費用対効果は良好であると結論づけた。その結果、65歳以上の成人についてはPPSV23の接種を継続するとした31)。
ドイツではSTIKO(Standing Committee on Vaccination)がワクチン接種の方針を決めている。STIKOはこれまでに発表された論文を精査し、PCV13-PPSV23連続接種は、予防可能症例数の増加分が少なく、NNV (Number needed to vaccinate;1人の肺炎による入院や死亡を防ぐために、何人にワクチンを接種する必要があるかを示す効果の指標)とコストが大きいことから、高齢者への標準ワクチンとして推奨しないとした32)。また、60歳以上の成人への標準ワクチンとしてはPPSV23の推奨を継続するとした。
フランスはハイリスク患者に肺炎球菌ワクチンを推奨しているが、65歳以上の成人にはとくに推奨はしていない33)。カナダとオーストラリアは65歳以上の成人にはPPSV23接種を推奨としており、以前の方針の変更はない34,35)。
以上のように現時点では上記の国々では、フランスを除いて65歳以上の成人にはPPSV23が推奨されている。各国とも定期接種としてのワクチン接種については、免疫原性、安全性、有効性、費用対効果等を評価し、各国の状況(患者数、血清型の分布、薬価など)により独自の方針が決められている。
(参考文献)
1) 第27回厚生科学審議会予防接種・ワクチン分科会予防接種基本方針部会 資料. (https://www.mhlw.go.jp/stf/newpage_03166.html)
2) Tomczyk S, Bennett NM, Stoecker C, Gierke R, Moore MR, Whitney CG, et al. Use of 13-valent pneumococcal conjugate vaccine and 23-valent pneumococcal polysaccharide vaccine among adults aged ≥65 years: recommendations of the Advisory Committee on Immunization Practices (ACIP). MMWR 2014;63(37):822-5.
3) 第24回厚生科学審議会予防接種・ワクチン分科会予防接種基本方針部会 資料.( https://www.mhlw.go.jp/content/10601000/000376443.pdf)
4) ACIP Live Meeting Archive-June 2019
(https://www.cdc.gov/vaccines/acip/meetings/live-mtg-2019-06.html)
5) 23価肺炎球菌莢膜ポリサッカライドワクチン(肺炎球菌ワクチン)ファクトシート.
(https://www.mhlw.go.jp/file/05-Shingikai-10601000-Daijinkanboukouseikagakuka-Kouseikagakuka/0000184910_1.pdf#search=%27 )
6) Suzuki M, Dhoubhadel BG, Ishifuji T, Yasunami M, Yaegashi M, Asoh N, et al. Serotype-specific effectiveness of 23-valent pneumococcal polysaccharide vaccine against pneumococcal pneumonia in adults aged 65 years or older: a multicenter, prospective, test-negative design study. Lancet Infect Dis. 2017; 17:313-21.
7) 新橋玲子、福住宗久、島田智恵、大石和徳、常 彬、鈴木 基.成人侵襲性肺炎球菌感染症に対する23価肺炎球菌莢膜ポリサッカライドワクチンの有効性.2018; IASR 39:115-6.
8) 定期の予防接種実施者数(http://www.mhlw.go.jp/topics/bcg/other/5.html).
9) Jackson LA, Gurtman A, van Cleeff M, Jansen KU, Jayawardene D, Devlin C, et al. Immunogenicity and safety of a 13-valent pneumococcal conjugate vaccine compared to a 23-valent pneumococcal polysaccharide vaccine in pneumococcal vaccine naive adults. Vaccine.2013;31:3577–84.
10) Jackson LA, Gurtman A, Rice K, Pauksens K, Greenberg RN, Jones TR, et al. Immunogenicity and safety of a 13-valent pneumococcal conjugate vaccine in adults 70 years of age and older previously vaccinated with 23-valent pneumococcal polysaccharide vaccine. Vaccine. 2013;31:3585–93.
11) Namkoong H, Funatsu Y, Oishi K, Akeda Y, Hiraoka R, Takeshita K, et al. Comparison of the immunogenicity and safety between polysaccharide and protein-conjugated pneumococcal vaccines among the elderly aged 80 years or older in Japan: An open-labeled randomized study. Vaccine. 2015;33(2):327-32. doi: 10.1016/j.vaccine.2014.11.023. Epub 2014 Nov.
12) Bonten MJ, Huijts SM, Bolkenbaas M, Webber C, Patterson S, Gault S, et al. Polysaccharide conjugate vaccine against pneumococcal pneumonia in adults. N Engl J Med. 2015; 372:1114-25.
13) Shimbashi R, Chang B, Tanabe Y, Takeda H, Watanabe H, Kubota T, et al. Epidemiological and clinical features of invasive pneumococcal disease caused by serotype 12F in adults, Japan. PLoS ONE 2019 Feb 21;14(2):e0212418. doi: 10.1371/journal.pone.0212418.
14) Ubukata K, Takata M, Morozumi M, Chiba N, Wajima T, Hanada S, et al. Effects of pneumococcal conjugate vaccine on genotypic penicillin resistance and serotype changes, Japan, 2010-2017. Emerg Infect Dis. 2018;24(11):2010-20.
15) Sando E, Suzuki M, Furumoto A, Asoh N, Yaegashi M, Aoshima M, et al. Impact of the pediatric 13-valent pneumococcal conjugate vaccine on serotype distribution and clinical characteristics of pneumococcal pneumonia in adults: The Japan Pneumococcal Vaccine Effectiveness Study (J-PAVE), Vaccine 2019; 37: 2687-93.
16) Akata K, Chang B, Yatera K, Kawanami T, Naito K, Noguchi S, et al. The distribution and annual changes in the Streptococcus pneumoniae serotypes in adult Japanese patients with pneumococcal pneumonia from 2011 to 2015. J Infect Chemother. 2017; 23:301-6.
17) Noguchi S, Yatera K, Akata K, Chang B, Ikegami H, Hata R, Yamasaki K, et al. Distribution and annual changes in the Streptococcus pneumoniae serotypes in Japanese adults with pneumococcal pneumonia from 2011 to 2017.J Infect Chemother. 2019;25:925-9.
18) Falkenhorst G, Rechmidt C, Harder T, Wichmann O, Glodny S, Hummers-Pradier E, et al. Bacground paper to the updated pneumococcal vaccination recommendation for older adults in Germany. Bundesgesundheitsblatt Gesundheitsforschung Gesundheitsschutz.2016; 59:1623-57.
19) Kobayashi M. Intervals between PCV13 and PPSV23 Vaccines: evidences supporting currently recommended intervals and proposed changes.MMWR 2015; 64(34):944-7.
20) Stoecker C, Kim L, Gierke R, Pilishvili T. Incremental Cost-Effectiveness of 13-valent Pneumococcal Conjugate Vaccine for Adults Age 50 Years and Older in the United States. J Gen Intern Med. 2016;31:901-8.
21) Black CL, Williams WW, Warnock R, Pilishvili T, Kim D, Kelman JA. Pneumococcal vaccination among Medicare Beneficiaries Occurring after the Advisory Committee on Immunization Practices Recommendation for routine use of 13-valent pneumococcal conjugate vaccine and 23-valent pneumococcal polysaccharide vaccine for adults aged ≥65 years. MMWR 2017; 66(27):728-33.
22) ACIP Presentation slides: June 2019. Pneumococcal(https://www.cdc.gov/vaccines/acip/meetings/slides-2019-06.html)
23) 一般社団法人日本感染症学会.肺炎球菌ワクチン再接種問題検討委員会.肺炎球菌ワクチン再接種のガイダンス(改訂版).感染症誌.91;4: 543-52.https://www.kansensho.or.jp/uploads/files/guidelines/pneumococcus_vaccine_re_1707.pdf
24) Greenberg RN, Gurtman A, Frenck RW, Strout C, Jensen KU, Trammel J, et al. Sequential administration of 13-valent pneumococcal conjugate vaccine and 23-valent pneumococcal polysaccharide vaccine in pneumococcal vaccine–naïve adults 60–64 years of age. Vaccine 2014;32:2364–74.
25) Jackson LA, Gurtman A, van Cleeff M, Frenck RW, Treanor J, Jansen KU, et al. Influence of initial vaccination with 13-valent pneumococcal conjugate vaccine or 23-valent pneumococcal polysaccharide vaccine on anti-pneumococcal responses following subsequent pneumococcal vaccination in adults 50 years and older. Vaccine.2013;31:3594–602.
26) de Roux A, Schmöle-Thoma B, Siber GR, HAckell JG, Kuhnke A, Ahlers N, et al. Comparison of pneumococcal conjugate polysaccharide and free polysaccharide vaccines in elderly adults: conjugate vaccine elicits improved antibacterial immune responses and immunological memory. Clin Infect Dis.2008;46(7):1015-23.
27) Goldblatt D, Southern J, Andrews N, Ashton L, Burbidge P, Woodgate S, et al. The immunogenicity of 7-valent pneumococcal conjugate vaccine versus 23-valent polysaccharide vaccine in adults aged 50–80 years. Clin Infect Dis.2009; 49:1318–25.
28) Miernyk KM, Butler JC, Bulkow LR, Singleton RJ, Hennessy TW, Dentinger CM, et al. Immunogenicity and reactogenicity of pneumococcal polysaccharide and conjugate vaccines in Alaska Native adults 55–70 years of age. Clin Infect Dis.2009; 49:241–8.
29) Hammitt LL, Bulkow LR, Singleton RJ, Nuorti JP, Hummel KB, Miernyk KM, et al. Repeat revaccination with 23-valent pneumococcal polysaccharide vaccine among adults aged 55–74 years living in Alaska: no evidence of hyporesponsiveness. Vaccine. 2011;29(12):2287–95.
30) Use of 13-valent pneumococcal conjugate vaccine and 23-valent pneumococcal polysaccharide vaccine for adults with immunocompromising conditions: recommendations of the Advisory Committee on Immunization Practice (ACIP). MMWR 2012;61: 816-9.
31) Interim JCVI statement on adult pneumococcal vaccination in the UK.
https://www.gov.uk/government/uploads/system/uploads/attachment_data/file/477966/JCVI_pnemococcal.pdf
32) Falkenhorst G, Remschmidt C, Harder T, Wichmann O, Glodny S, Hummers-Pradier, et al. Background paper to the updated pneumococcal vaccination recommendation for older adults in Germany. Bundesgesundheitsblatt Gesundheitsforschung Gesundheitsschutz 2016;59 (12): 1623-57.
33) Calendrier des vaccinations et recommandations vaccinales 2017.
http://social-sante.gouv.fr/prevention-en-sante/preserver-sa-sante/calendrier-vaccinal(updated April 2017)
34) Canadian Immunization Guide: Part 4 - Active Vaccines. https://www.canada.ca/en/public-health/services/publications/healthy-living/canadian-immunization-guide-part-4-active-vaccines/page-16-pneumococcal-vaccine.html
35) The Australian Immunisation Handbook. Pneumococcal diseases. https://immunisationhandbook.health.gov.au/vaccine-preventable-diseases/pneumococcal-disease(updated 20 September 2019)
2019年10月30日
日本呼吸器学会呼吸器ワクチン検討WG委員会/日本感染症学会ワクチン委員会・合同委員会
(大石和徳※、西順一郎※※、岩田 敏、岡田賢司、神谷 元、川名 敬、関 雅文、多屋馨子、
朝野和典、永井英明、中野貴司、中村茂樹、丸山貴也、宮下修行、迎 寛、渡辺 彰)
※日本呼吸器学会呼吸器ワクチン検討WG委員会委員長
※※日本感染症学会ワクチン委員会委員長









